_______________________________________________________
3 Emofiltrazione continua in rianimazione
_______________________________________________________
Amedeo Pignataro -
Servizio di Anestesia e Rianimazione Ospedale Buccheri la Ferla
di palermo - Italia e-mail: pignata@tin.it
Le metodiche di depurazione extra-renale (emodialisi, emofiltrazione, dialisi peritoneale), supporto fondamentale per i pazienti uremici, sono spesso poco tollerate dai pazienti critici che sviluppano un'insufficienza renale acuta durante un ricovero in terapia intensiva; perturbazioni emodinamiche e idroelettrolitiche da un lato, e problemi tecnici legati alla complessità delle procedure depurative dall'altro, rendono, infatti, tali metodiche inapplicabili in rianimazione. In seguito alle prime esperienze cliniche negli anni '70, con l'emofiltrazione artero-venosa continua (CAVH) in pazienti con sovraccarico idrico resistente ai diuretici, le tecniche "sostitutive" renali continue hanno trovato una sempre maggiore applicazione in terapia intensiva, fino a divenire un trattamento di routine in questo settore.
L'esperienza dell'unità di terapia
intensiva dell'ospedale Buccheri La Ferla F.B.F. di Palermo nasce
nell'anno 1993 con l'impiego dell'emofiltrazione artero-venosa
continua (CAVH) per il trattamento dell'insufficienza renale acuta
di pazienti con insufficienza cardiaca, sepsi, politrauma. Uno
stage del personale medico-infermieristico presso un centro di
dialisi, permetteva la graduale sostituzione della CAVH con l'emofiltrazione
veno-venosa continua (CVVH), effettuata con un apparecchio d'emofiltrazione
"intermittemte" modificato. Ad oggi su 700 ricoveri
in terapia intensiva, la CVVH è stata praticata in 70 pazienti.
Le tecniche di depurazione extrarenale
continua (CRRT=Continuous Renal Replacement Therapies) comprendono,
oltre l'emofiltrazione continua artero-venosa e veno-venosa, anche
l'emodialfiltrazione continua artero-venosa (CAVHD) e veno-venosa
(CVVHD).
| Emodinamicamente ben tollerate |
| Minime alterazioni dell'osmolarita' plasmatica |
| Migliore controllo di azotemia, elettroliti ed EAB |
| Altamente efficaci nella rimozione di liquidi |
| Correzione di eventuali alterazioni in corso di trattamento |
| Contemporanea somministrazione di liquidi, tpn, farmaci |
| Procedure tecnicamente semplici |

L'emofiltrazione, diversamente dall'emodialisi, che sfutta il principio della diffusione, è basata sulla convezione, secondo la quale i soluti disciolti in un soluto si spostano, secondo un gradiente di concentrazione, da un settore in cui la pressione è più elevata ad un altro in cui essa è minore. Non appena il sangue attraversa l'emofiltro, un gradiente di pressione transmembrana (TMP) tra il compartimento ematico e quello dell''ultrafiltrato determina la filtrazione della quota idrica ematica attraverso la membrana altamente permeabile del filtro. Il movimento dell'acqua veicola piccole e grandi molecole lungo la membrana depurando il sangue. La quantità di filtrato (Quf) prodotta dipende da alcuni fattori secondo l'equazione:
| Quf = CH2O x S x TMP |
Dove CH2O è il coefficiente
di permeabilità idraulica della membrana, S la superficie
della membrana e TMP la pressione transmembrana, ovvero la risultante
tra la pressione idrostatica e oncotica ai due lati della membrana
del filtro. Nella figura è mostrato l'influenza del flusso
ematico (Q) e della pressione transmembrana sulla produzione di
ultrafiltrato.

Una caratteristica interessante dell'emofiltrazione
è la capacità di rimuovere dal sangue molecole di
medie dimensioni (2000-30000 Da), altrimenti non dializzabili
per via della loro bassa concentrazione ematica. Tale caratteristica
è il presupposto fondamentale per l'impiego dell'emofiltrazione
nella sepsi.
|
|
|
|
|
|
Negli ultimi anni, numerosi autori hanno indicato le CRRT (emofiltrazione/emodiafiltrazione) come strumenti potenziali per l'epurazione delle sostanze liberate nell'organismo durante la sepsi (1,2), l'ARDS (3) o la MOF.
Tali sostanze, ovvero i mediatori dell'infiammazione, comprendono le frazioni del complemento attivato (C3a, C5a), i metaboliti dell'acido arachidonico, le chinine, il fattore attivante le piastrine (PAF), le citokine (TNF, IL), le proteasi ed altre non ancora identificate. Numerosi lavori, condotti nell'animale e nell'uomo, volti a studiare la clearance della CRRT nei confronti di tali mediatori, hanno dato risultati incoraggianti (4, 5, 6, 7). Se, tuttavia, è possibile stabilire una relazione tra la mortalità dei pazienti settici e il tasso di citokine circolanti, non è certo che la rimozione di tali sostanze possa portare necessariamente ad una riduzione della mortalità. E' probabile che altre sostanze ancora sconosciute intervengano nel mantenimento della sepsi e questo potrebbe giustificare l'altissima mortalità di questa sindrome, nonostante i supporti ventilatori, emodinamici e depurativi fino ad oggi attuati.
L'emofiltrazione continua può essere attuata tramite un circuito artero-venoso (CAVH = continuous arterio-venous haemifiltration), o veno-venoso (CVVH = continuous veno-venous haemofiltration).
La CAVH, è una tecnica che non necessita di materiale complesso, è semplice da eseguire e può pertanto essere utilizzata da equipe senza esperienze precedenti con le tecniche depurative extrarenali, o in caso d'indisponibilità d'apparecchi d'emofiltrazione veno-venosa per la presenza di più pazienti in trattamento emofiltrativo. La CAVH che sfrutta la pressione arteriosa del paziente come "motore" del circuito, consiste di una cannula arteriosa, un circuito venoso, un filtro, un sistema di raccolta dell'ultrafiltrato, un circuito venoso e una cannula venosa. Il circuito è dotato anche di un sistema per l'anticoagulazione.
La CAVH, in quanto regolata dalla pressione arteriosa del paziente, non permette, in caso di gravi ipotensioni, la rimozione di grosse quantità di soluti; il volume orario di filtrato ottenibile con tale metodica, nonostante l'elevata permeabilità dei filtri disponibili, non si rivela sufficiente nel trattamento di malati settici e ipercatabolici. L'incostante flusso plasmatico attraverso il filtro richiede, inoltre, una generosa anticoagulazione per minimizzare la formazione di coaguli nel circuito. Il ricorso ad un accesso arterioso di grosso calibro, necessario per assicurare un flusso ematico di circa 50 ml/min, impone nella CAVH il posizionamento di grosse cannule arteriose (soprattutto femorali) con gli evidenti rischi di ematomi, emorragie, laceramenti vascolari, trombosi.
L'inclusione di una pompa sangue nel circuito d'emofiltrazione, come avviene nella CVVH, garantendo un flusso ematico stabile, permette di aumentare il volume di ultrafiltrato prodotto (oltre 24 litri/die) e la clearance di grosse quantità di urea e creatinina, in tal modo eliminando la pressione arteriosa del pz. come motore del circuito. La rimozione lenta e continua dei cataboliti, necessitando di periodi prolungati (36-48 ore e più), peraltro, permette di evitare le rapide variazioni emodinamiche e di osmolarità tipiche dell'emofiltrazione e dell'emodialisi intermittente. La necessità di garantire un flusso di sangue ottimale, soprattutto nei pazienti ipotesi, richiede nella CAVH il posizionamento di grosse cannule arteriose (soprattutto femorali) con gli evidenti rischi di ematomi, emorragie, laceramenti vascolari, trombosi. Nella CVVH, l'uso di cateteri a doppio lume in una vena centrale rende più semplice e meno rischioso il problema dell'accesso vascolare.
Tutte le metodiche di depurazione extrarenale, esponendo il sangue a materiali esogeni di natura diversa rispetto all'endotelio vascolare, determinano l'attivazione dell'emostasi. L'emofiltrazione, pertanto deve prevedere un sistema di anticoagulazione che può essere attuato utilizzando diverse sostanze (eparina non frazionata, citrato, prostaciclina). L'eparina non frazionata è l'anticoagulante più utilizzato nelle CRRT. L'infusione continua, piuttosto che l'iniezione di boli ripetuti, è il sistema che permette di ottenere i migliori risultati.
La quantità di eparina/ora dipende da fattori legati al paziente e alla sua patologia ma anche dalla necessità, durante le techiche di depurazione continua, di garantire un trattamento prolungato. All'interno del filtro, inoltre, l'emoconcentrazione aumenta la quantità di fattori della coagulazione a contatto con la membrana, riducendo nel tempo la performance del sistema ed esponendo al rischio d'ostruzione. Il flusso sanguigno è un altro elemento importante: minore è il flusso, maggiore è il tempo di contatto del sangue con la membrana del filtro con conseguente aumento della formazione di coaguli.
La velocità dell'eparina va regolata, pertanto, non al raggiungimento di valori coagulativi rigidi, ma, in relazione all'assetto coagulativo del paziente e all'ovvio bisogno di evitare la formazione di coaguli nel circuito extracorporeo. Come regola generale, si può iniziare con un bolo (10-50 UI/kg) seguito da un'infusione continua di 5-20 UI/kg/h di eparina, monitorizzando ogni 8-12 ore il PTT. Un accorgimento che può ridurre la formazione di coaguli é l'infusione del liquido di restituzione secondo il metodo pre-diluizionale (prima del filtro). La riduzione della concentrazione dei soluti plasmatici all'entrata del filtro e, di conseguenza la loro clearance, è minimizzata dall'uso di grossi volumi di scambio. Al contrario, con il metodo post-diuizionale pur aumentando l'efficacia della filtrazione, soprattutto per più di 10 litri/die di ultrafiltrato, si ottiene un sangue troppo viscoso nel filtro con maggior rischio di coaguli.
Il monitoraggio dell'emofiltrazione s'indirizza al controllo dei parametri emodinamici (ipo-, ipertensione, aritmie), respiratori (sovraccarico idrico), dell'equilibrio idro-elettrolitico, acido-base e dell'osmolarità plasmatica. Allo stesso modo va eseguito il monitoraggio (ogni 8-12) della funzionalità renale e metabolica (creatinina, azotemia) e dell'assetto coagulativo (piastrine, AP, PTT). La determinazione degli elettroliti, azoto, creatinina nel filtrato è un indicatore utile per l'efficienza dell'emofiltrazione. I volumi scambiati ed il rapporto tra ultrafiltrato e soluzione di restituzione va determinato in base alla quantità di azoto e creatinina nel sangue prima della depurazione e al valore che si desidera raggiungere, alle condizioni emodinamiche ed idroelettrolitiche.
La dispersione termica del circuito
d'emofiltrazione può essere responsabile di gravi ipotermie:
a questo scopo, se nell'apparecchio emofiltrativo non è
previsto un sistema di riscaldamento del sangue è oppurtuno
adattare provvedimenti per minimizzare la dispersione del calore.
Nella nostra esperienza usiamo avvolgere il filtro e la circuiteria
con materiale isolante (fogli di alluminio).
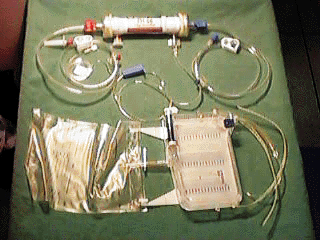
MONTAGGIO E PROCEDURE D'USO DELL'EMOFILTRAZIONE VENO-VENOSA CONTINUA (CVVH).

|

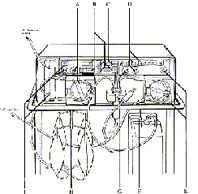
L'apparecchio mostrato in figura è previsto per l'emofiltrazione intermittente, mentre per effettuare l'emofiltrazione veno-venosa continua è necessario disattivare il modulo inferiore (mod. ultrafiltrato) e utilizzare solamente il modulo superiore (mod. sangue).
Questo è reso possibile dalla sostituizione dello spinotto d'alimentazione originale (tipo SCART), situato nel pannello posteriore del modulo sangue, con un'altro spinotto che esclude il collegamento tra i 2 moduli e permette l'alimentazione elettrica del solo modulo sangue.
1. MATERIALI:
| B. FILTRO PER EMOFILTRAZIONE GAMBRO FH 88 H. |
| C. LINEA ARTERIOSA A300B8H |
| D. LINEA VENOSA V200XD |
| E. N. 2 POMPE VOLUMETRICHE (ABBOTT LIFECARE 5000) CON RELATIVI DEFLUSSORI |
| F. N. 3 FLEBO DA 500 ML DI SOL. FISIOLOGICA |
| G. SACCA/E (4.5 L.) D'EMOFILTRAZIONE |
| H. CANNULA VENOSA A DOPPIO LUME |
| I. N. 2 KLEMMER O PINZE PER CLAMPARE |
A. Aggiungere 1 ml di eparina in 2 flebo da 500 ml di sol. Fisiologica; la terza flebo non va eparinizzata
B. Diluire in siringa da 50 ml 1 ml di eparina con 49 ml di sol. Fisiologica.
C. Fissare il filtro nell'apposito supporto dell'apparecchio sempre con l'estremita' arteriosa (quella lontana dall'uscita del filtrato) rivolta in basso.
D. Introdurre lo spike della linea arteriosa (colore rosso) nella flebo non eparinizzata;
E. Posizionare la linea art. Nell'apparecchio seguendo le frecce disegnate (clamp art.->trasduttore press. Art.->pompa sangue (ruotare la pompa solo in senso antiorario) ->estremita' art. Filtro
F. Collegare l'estremita' della linea arteriosa al filtro (raccordo luer-lock).
F. Inserire la camera di rivelazione d'aria nell'apposito sostegno in alto a sn. Dell'apparecchio.
G. Connettere il raccordo dotato di filtro al trasduttore di pressione.
H. Inserire la linea venosa (colore blu) nella clamp venosa, seguendo la freccia vedi figura); l'estremita' opposta della linea (lato pz.), Durante il riempimento del circuito va posta nel bidone di raccolta (per il tramite del raccordo a "v" presente nella confezione e che si avrà cura di conservare sterilmente).
I. Collegare la linea ultrafiltrato (in sostituzione il raccordo della sacca per tpn) all'uscita laterale del filtro. Per collegare l'estremità opposta della linea al deflussore della pompa abbott, è necessario tagliare la linea dopo circa 10 cm dal raccordo filtro. Il suddetto deflussore va collegato alla pompa abbott e successivamente all'urometro.
L. Collegare il 2° deflussore alla sacca d'emofiltrazione e in seguito alla 2a pompa abbott; l'estremità opposta del deflussore va connessa alla linea arteriosa prima del filtro o alla venosa dopo il filtro (direttamente alla camera di rivelazione d'aria o all'entrata della via venosa).
M. Connettere la siringa con l'eparina al raccordo presente sulla linea arteriosa e collegarla all'apposita pompa del modulo dell'apparecchio.
A. Accendere l'interruttore generale dell'apparecchio.
B. Premere il "silenzia allarme" e "riv. D'aria disattiv." per avviare il circuito.
C. Togliere la clamp dall'estremita' art. innestata alla sol. Fis. non eparinizzata e accendere ruotando la pompa sangue (manopola verde) fino ad una velocita' di 50-100 ml/min.
D. Durante il riempimento rimuovere le bolle d'aria dal circuito
E. Prima di innestare la 2a flebo (eparinata), spegnere la pompa sangue e clampare la linea art. al di sotto dello spike.
F. Dopo avere riempito il circuito con 1000 ml di sol. Fis. clampare la via venosa subito dopo il filtro e attivare la pompa abbott, per permettere il riempimento della linea ultrafiltrato (durante questa manovra è necessario fare uscire l'aria presente nel deflussore innestando una siringa senza pistone nella via secondaria ).
G. Una volta riempito completamente il circuito, spegnere la pompa sangue, clampare le estremita' arteriosa e venosa e connettere al pz.
H. Prima di cominciare l'emofiltrazione, regolare gli allarmi di pressione venosa tra -50 e + 200 mmhg.
I. Riattivare il tasto "riv.d'aria riattiv" e "riv.d'aria disattiv."
A. Spegnere la pompa sangue.
B. Clampare le estremita' (art. e venosa) lato pz.
C. Collegare le 2 estremita' al raccordo a "v" presente nella confezione della linea venosa.
D. Accendere la pompa sangue a 50 ml/min.
A. Spegnere la pompa sangue.
B. Deconnettere l'estremita' art. Lato pz. , collegarla allo spike (quest'ultimo va conservato tappato alla fine della procedura di riempimento del circuito) e innestarlo in una flebo di sol. Fis. 250 ml.
C. Accendere la pompa sangue (velocita' 50 ml/min).
D. Per permettere una completa restituizione del sangue del circuito, lasciare penetrare nello stesso l'aria alla fine della flebo. All'arrivo dell'aria in prossimita' del filtro, capovolgerlo fino al recupero totale del sangue.
E. Spegnere la pompa sangue e contemporaneamente clampare l'estremita' venosa (lato pz.), Quando la camera rivelatrice d'aria si vuota completamente dal sangue.
6.1 come fare fouriuscire il sangue in eccedenza dalla camera rivelatrice d'aria
A. Prendere una siringa di 20 ml, togliere lo stantuffo e posizionare una garza sterile al suo interno.
B. Chiudere con una klemmer il raccordo di calibro maggiore presente sopra il rivelatore d'aria.
C. Connettere la siringa allo stesso raccordo.
D. Togliere la klemmer dal raccordo finche' non si e' raggiunto il livello desiderato.
E. Chiudere nuovamente il raccordo con la klemmer e togliere la siringa.
N.b. per questa procedura non e' necessario fermare il circuito.
A. Prendere una siringa di 20 ml, togliere lo stantuffo e posizionare una garza sterile al suo interno.
B. Chiudere con una klemmer il raccordo di calibro maggiore presente sopra il rivelatore d'aria.
C. Connettere la siringa allo stesso raccordo.
D. Chiudere con una 2a klemmer la linea venosa subito dopo il rivelatore d'aria ed aprire la klemmer del raccordo superiore, finche' il sangue non raggiunge il livello indicato dalla linea sulla camera .
E. Chiudere nuovamente con la klemmer il raccordo superiore e riaprire immediatamente quello inferiore.
F. Togliere la siringa e richiudere con un tappo sterile il raccordo.
N.b. per questa procedura non e' necessario fermare il circuito.
La CVVH, così com'è stata attuata finora, presenta alcuni limiti: anzitutto le pompe volumetriche da noi utilizzate, non permettono un flusso orario maggiore di 999 ml, sia per quanto riguarda il filtrato che il liquido di restituzione. L'esclusione del modulo dell'ultrafiltrato (vedi figura), inoltre, impedisce di utilizzare il sistema di riscaldamento della macchina, esponendo pertanto i pazienti all'ipotermia, tanto maggiore quanto più elevati sono gli scambi orari. Il modulo dell'emofiltrato presenta anche un sistema d'allarme per le perdite ematiche, qualora nel settore del filtrato comparisse sangue. Per tale motivo, recentemente la Gambro ha provveduto a modificare l'apparecchio per emofiltrazione, in modo tale da poter essere utilizzato a 2 moduli, mantenendo la possibilità di lavorare a bassi flussi di ultrafiltrato (15 ml/min). La modifica prevede, infatti, l'aggiunta di un "selettore" di velocità nel modulo emofiltrato, che consente di regolare la velocità della pompa del filtrato da 1 (15 ml/min) a 6 (100 ml/h).
Recenti lavori sperimentali, condotti
da Grootendorst, hanno dimostrato l'effetto positivo dell'aumento
del volume di ultrafiltrazione durante CRRT, in animali ai quali
veniva indotto uno shock settico. Un'evoluzione delle tecniche
abituali di CRRT ha condotto a nuove applicazioni che sono state
definite emofiltrazione ad alti volumi (HVHF): con questo termine
si fa riferimento a tecniche in grado di produrre più di
75 litri di ultrafiltrato al giorno. In pratica lo scopo può
essere raggiunto o mantenendo una produzione di ultrafiltrato
superiore a 4 l/ora oppure inserendo in una metodica d'emofiltrazione
continua classica, un periodo di alcune ore condotto con volumi
d'ultrafiltrato maggiori di 8 l/ora. Nonostante le prime esperienze
cliniche (8),
la tollerabilità per i pazienti e la fattibilità
della HVHF sono ancora da dimostrare.
_______________________________________________________
4 Manuali di Anestesia: Anestesia in chirurgia addominale - Pancreasectomia: resezione sec. Wipple
________________________________________________________
Questa rubrica, curata dal dott. Lelio Guglielmo,presenta i protocolli anestesiologici adottati ,nelle varie specialitàchirurgiche , dal Servizio di Anestesia e Rianimazione dell' OspedaleBuccheri La Ferla. Questi manuali che sono il frutto di studie dell'esperienza di oltre 15 anni di attività anestesiologicanon pretendono ovviamente di avere un carattere "universale". E' evidente altresì che l'applicazione delle proceduredescritte va valutata criticamente in relazione al proprio ambientedi lavoro. La parte riguardante le considerazioni chirurgicheè stata realizzata in collaborazione con i chirurghi dellevarie specialità, operanti nel nostro ospedale.
Qualsiasi commento o critica èbene
accetta e deve essere inviata a leliobuc@mbox.vol.it. oppurealla
redazione LANZA@mbox.unipa.it
|  |
| Considerazioni chirurgiche
La pancreasectomia distale viene eseguita per i tumori della metà distale del pancreas. Il peritoneo viene inciso lungo la superfice inferiore del pancreas, avendo cura di evitare la lacerazione dei vasi del colon trasverso.Successivamente segue la mobilizzazione della milza; l'arteria splenica viene legata a livello della sua origine. Il legamento gastro-splenico viene reciso, i vasi gastrici brevi e la gastroepiploica di sinistra vengono legati. La vena mesenterica inferiore viene legata lungo il margine inferiore del pancreas, e la vena splenica è legata a livello del punto di sezione prefissato. Il pancreas sezionato viene solitamente suturato ed il dotto viene legato. La milza può essere conservata quando non ci siano neoplasie, purchè i vasi splenici siano legati prossimalmente all'ilo al fine di preservare il circolo collaterale. Varianti di procedure o approcci: La Pancreasectomia subtotale solitamente implica la sezione del pancreas distalmente ai vasi mesenterici, lasciando la testa ed il processo uncinato intatti. Questa tecnica può essere utilizzata per tumori o pancreatite cronica. La tecnica di Child consiste nella rimozione di tutto il pancreas eccetto un margine di tessuto lungo l'ansa del duodeno; in questo modo non è necessario, avendo preservato il duodeno, ricostruire la via biliare. Tale tecnica è di solito riservata ai pazienti con pancreatite cronica. Diagnosi preoperatorie abituali: Carcinoma del pancreas; pancreatite cronica; tumori delle cellule insulari. Resezione secondo Wipple La resezione secondo Whipple consiste di una duodenopancreasectomia, seguita da un'anastomosi del moncone pancreatico distale col digiuno, una coledocodigiunostomia, ed una gastrodigiunostomia (vedi figura sotto).Visualizzata la cavità peritoneale si decide l'operabilità della lesione. Le controindicazioni alla resezione comprendono: il coinvolgimento dei vasi mesenterici superiori; l'infiltrazione del tumore alla base del mesentere, l'estensione all'ilo epatico con interessamento dell'arteria epatica; metastasi epatiche.Giudicato operabile il tumore, viene attuata una ulteriore mobilizzazione della testa del pancreas. Il dotto epatico comune viene sezionato al disopra dell'insorgenza del cistico e viene rimossa la colecisti. Una volta che la vena mesenterica superiore è stata isolata dal pancreas, quest'ultimo viene sezionato avendo cura di non danneggiare la vena splenica. Lo stomaco viene sezionato a livello della giunzione tra corpo e antro, oppure oltre il piloro, nel caso in cui non sia coinvolto dal tumore. Il digiuno è sezionato al di là del Treitz ed il moncone prossimale rimosso dopo aver separato le connessioni vascolari coi vasi mesenterici. La ricostruzione è ottenuta anastomizando il moncone pancreatico distale, la via biliare e lo stomaco al digiuno.Vengono posizionati dei drenaggi nei pressi dell'anastomosi pancreatica. Varianti di procedure o approcci: Esistono diverse varianti che riguardano l'estensione della tecnica secondo Whipple: la pancreasectomia totale, la pancreasectomia regionale, che comprendono la resezione e la ricostruzione della vena e/o dell'arteria mesenterica superiore retropancreatica; e la resezione pancreatica senza interessamento del piloro. Diagnosi preoperatorie abituali: carcinoma del pancreas; cistoadenomi maligni; pancreatite cronica. | |

Cenni anatomici |  Intervento di Wipple |
| WHIPPLE | PANCREASECTOMIA | |
| Posizione | supina | supina |
| Incisione | mediana | mediana |
| Strumenti speciali | retrattore di Denier | lo stesso |
| Antibiotico | ceftriaxone | lo stesso |
| T.chirurgico | 4-6 h | 3-5 h |
| Perdite sangue | 500 ml | 750-1000 ml |
| Mortalità | 5-8% | 10-15% |
| Morbidità | Ritardato svuotamento gastrico : 25%
Sepsi :5-15% Emorragia : 5% Infarto mioc. : 1-3% Fistola biliare : <2% Fistola pancreatica : 3-5% | lo stesso 5% <5% 1-3% <1% |
| Pain score | 7-9 | 7-9 |
| CONSIDERAZIONI ANESTESIOLOGICHE PER LA CHIRURGIA DEL PANCREAS |
| PREOPERATORIO I pazienti da sottoporre a chirurgia del pancreas possono essere tipicamente divisi in tre gruppi: 1) Pazienti con pancreatite cronica che non hanno giovato della terapia medica. Tali soggetti possono presentarsi al tavolo operatorio in condizioni critiche per una riacutizzazione della pancreatite o per un dubbio diagnostico. 2) Pazienti con carcinoma pancreatico, comprendendo i tumori ormonosecernenti come l'insulinoma o il gastrinoma (S. di Zollinger-Ellison). 3) Pazienti da trattare per le sequele della pancreatite cronica come ad es.pseudocisti o ascessi. |
| App. Respiratorio: Una compromissione anche grave, dovuta ad es. a versamenti pleurici, atelettasie, ARDS, che progrediscono verso l'insufficenza respiratoria, può essere presente anche nel 50% dei soggetti con pancreatite acuta. Per tali soggetti sarà necessario un certo periodo di ventilazione meccanica nel postoperatorio. Tests necessari: Rx torace, EGA. |
| App. Cardiovascolare: I pazienti con pancreatite acuta possono essere ipotesi e richiedere una notevole quantità di liquidi ed albumina per il ripristino della volemia prima dell'intervento chirurgico.Si possono anche notare modificazioni dell'ECG che simulano l'ischemia miocardica. La pancreatite acuta ed i tumori ormonosecernenti si caratterizzano anche per notevoli squilibri elettrolitici: la riduzione del potassio può essere grave e deve essere corretta possibilmente nel preoperatorio.Tests necessari: ECG, elettroliti. |
| App. Gastrointestinale: Ittero e dolore addominale sono sintomi frequenti in tale popolazione di pazienti. La presenza di un ileo paralitico o di un'occlusione meccanica richiederà la messa in opera delle precauzioni necessarie per i paz. a stomaco pieno. Squilibri idrolettrolitici sono frequenti in corso di pancreatite acuta e possono comprendere un'alcalosi metabolica ipocloremica, ipocalcemia, ipomagnesemia, iperglicemia. Tali squilibri andrebbero corretti nel preoperatorio. La S. di Zollinger-Ellison si accompagna a diarrea e malattia ulcerosa peptica grave, spesso complicata da perforazione o sanguinamento. I Vipomi determinano una massiva diarrea acquosa e squilibri idroelettrolitici.
Tests necessari: Elettroliti, glicemia, calcemia, amilasi, tgo/p,bil.totale ed indiretta |
| Rene: I pazienti possono presentare insufficenza renale e, in questo caso, il protocollo anestesiologico va modificato.
Tests: azotemia,creatinina,ecc.. |
| Sistema Endocrino: Molti pazienti con pancreatite acuta possono presentare un diabete di II tipo secondario alla perdita di tessuto pancreatico. I tumori ormonosecernenti del pancreas sono occasionalmente associati a sindromi paraneoplastiche (MEN-I; paratiroide, pancreas, ipofisi, e feocromocitomi). L'insulinoma è il più comune tumore ormonosecernete del pancreas e può determinare ipoglicemia. Sono necessari destrostix ripetuti e profili glicemici. |
| Sangue: L'ematocrito può essere falsamente elevato per effetto di emoconcentrazione, oppure basso per un'emorragia. Può presentarsi una coagulopatia.Tests: CBG ; piastrine, PT, PTT e fibrinogeno. Richiesta di sangue ed emoderivati: 2-3 unità di emazie concentrate; prevedere utilizzazione di piastrine e PFC nel postoperatorio immediato
Premedicazione della veglia: se le condizioni cliniche lo consentono somministrare Tavor 1-2mg la sera alle 22 e la mattina alle 6. |
INTRAOPERATORIO
| Emodiluzione | secondo standard |
| Monitoraggio | ECG,Pa cruenta, capnografia, SaO2, doppler esofageo, diuresi oraria. |
| Accessi vascolari | 2 v.periferiche + 1 v.centrale |
| Tecnica di anestesia | AG+AP se le condizioni della volemia lo consentono ed il paziente non è occluso. Se il paziente è ipovolemico andrà ripristinata la volemia (colloidi, albumina,cristalloidi o sangue) prima dell'induzione, e andranno rivisti i dosaggi degli analgesici e ipnotici da somministrare.I liquidi da infondere vanno tutti riscaldati. |
| Mantenimento | propofol+remifentanil (se Ag pura). Propofol + bupivacaina 0.3% a 6 ml.hr per via peridurale (se AG+AP).Evitare il protossido se è presente distensione intestinale. |
| Dobutamina | secondo protocollo |
| Risveglio | generalmente in UTIR. Il paz. verrà mantenuto in VAM sino a stabilizzazione completa delle condizioni emodinamiche e respiratorie. |
| Complicanze | Ipokaliemia e Ipovolemia. La maggior parte della chirurgia del pancreas è associata a grandi spostamenti e perdite di liquidi. Il rilascio di lipasi pancreatiche e la conseguente saponificazione del grasso omentale comportano una grave ipocalcemia. Una grave emorragia può verificarsi durante la dissezione del pancreas dai vasi portali e mesenterici. |
POSTOPERATORIO
| Complicanze: Squilibri idroelettrolitici; Ipovolemia; Ipotermia; Ipocalcemia; Iperglicemia.
La pancreasectomia totale si accompagna ad un diabete che può essere molto difficile da controllare. La resezione subtotale comporta una iperglicemia variabile. Analgesia post.op.: Peridurale continua con Marc.0.3% a 6-9ml/hr +Meperidina 50mg.IM ogni 4-6 ore. PCA con morfina se in UTIR |
-----------------------------------------------------------------------------------------
Informazioni sulla rivista
EDUCATIONAL SYNOPSES IN ANESTHESIOLOGY
and
CRITICAL CARE MEDICINE-Italia-
Educational Synopses in Anesthesia and Critical Care Medicine-Italia costituisce la parte Italiana della versione Americana, pubblicata su Internet da Keith J Ruskin, Professore di Anestesia alla Università di Yale. I lavori saranno accettati sia in lingua Italiana che Inglese. In quelli di lingua Italiana un corposo riassunto in Inglese verrà preparato dalla redazione, qualora l'autore non fosse in grado di fornirlo. A cura della redazione sarà inoltre la traduzione in Italiano dei manoscritti inviati in lingua Inglese. La rivista sarà inviata gratuitamente a tutti quelli che ne faranno richiesta inviando il seguente messaggio "Desidero ricevere ESIA versione italiana" indirizzato a LANZA@MBOX.UNIPA.IT
La rivista pubblica rewiews e lavori originali compiuti nei campi dell'anestesia e della medicina critica. I lavori originali riguardano ricerche cliniche, di laboratorio e la presentazione di casi clinici. Le reviews includono argomenti per l'Educazione Medica Continua (EMC), articoli di revisione generale o riguardanti le attrezzature tecniche. ESIA pubblicale lettere all'Editore contenenti commenti su articoli precedentemente publicati ed anche brevi comunicazioni. La guida per gli autori può essere consultata collegandosi al sito ANESTIT all'indirizzo:
http://www.unipa.it/~lanza
utilizzando la sezione riservata ad ESIA-Italia
Oppure può essere richiesta inviando un messaggio a
lanza@mbox.unipa.it
EDUCATIONAL SYNOPSES IN ANESTHESIOLOGY
and
CRITICAL CARE MEDICINE Sezione Italiana
E' anche ottenibile attraverso World-WideWeb WWW: L' URL per questo numero di ESIA è:
http://www.unipa.it/~lanza/esiait/esit9712.txt
Il nome della rivista è
esitaamm, dove aa è l'anno ed mm il mese
(per esempio questo numero èesit9712.txt)
LA REDAZIONE DI ESIA ITALIA
DIRETTORE
Vincenzo LANZA
Primario del Servizio d'Anestesia e Rianimazione Ospedale Buccheri La Ferla Fatebenefratelli
Palermo LANZA@MBOX.UNIPA.IT
Terapia Intensiva
Antonio Braschi
Primario del Servizio d'Anestesia e Rianimazione 1
Policlinico S. Matteo - IRCCS Pavia
Anestesia Cadiovascolare
Riccardo Campodonico
Responsabile dell'Unità di Terapia Intensiva Cardiochirurgica
Azienda Ospedaliera di Parma ricrob@mbox.vol.it
Anestesia e malattie epatiche
Andrea De Gasperi
Gruppo trapianti epatici / CCM
Ospedale Niguarda - Milano
Medicina critica e dell'emergenza
Antonio Gullo
Professore di Terapia Intensiva
Direttore del Dipartimento di Anestesia e Terapia Intensiva-Università di Trieste
Anestesia ed informatica
Vincenzo Lanza
Primario del Servizio d'Anestesia e Rianimazione Ospedale Buccheri La Ferla Fatebenefratelli
Palermo
Tosssicologia
Carlo Locatelli
Direttore del Centro di Informazione Tossicologica Centro antiveleni di Pavia
Fondazione Scientifica
"Salvatore Maugeri Clinica delLavoro e della Riabilitazione"
Pavia
Terapia Antalgica e Cure Palliative
Sebastiano Mercadante
Aiuto del Servizio d'Anestesia e Rianimazione
Ospedale Buccheri La Ferla Fatebenefratelli
Palermo